Identifican el doble efecto de la proteína C3G en el linfoma B: frena el tumor, pero favorece su expansión.
Investigadores del Centro de Investigación del Cáncer y del Instituto de Investigación Biomédica de Salamanca han descubierto que la proteína C3G desempeña un papel dual en el linfoma de células B: actúa como freno del crecimiento tumoral, pero al mismo tiempo favorece la diseminación del cáncer.
El trabajo, publicado en la revista Cell Communication and Signaling, ha sido codirigido por Carmen Guerrero y José María De Pereda, investigadores principales del Centro de Investigación del Cáncer, y se ha desarrollado mediante experimentos en modelos celulares y animales.
Según destaca Guerrero, “C3G podría servir como marcador para predecir si el linfoma se extenderá y convertirse en una diana para nuevos tratamientos que frenen el tumor sin favorecer las metástasis”.
Un interruptor molecular alterado
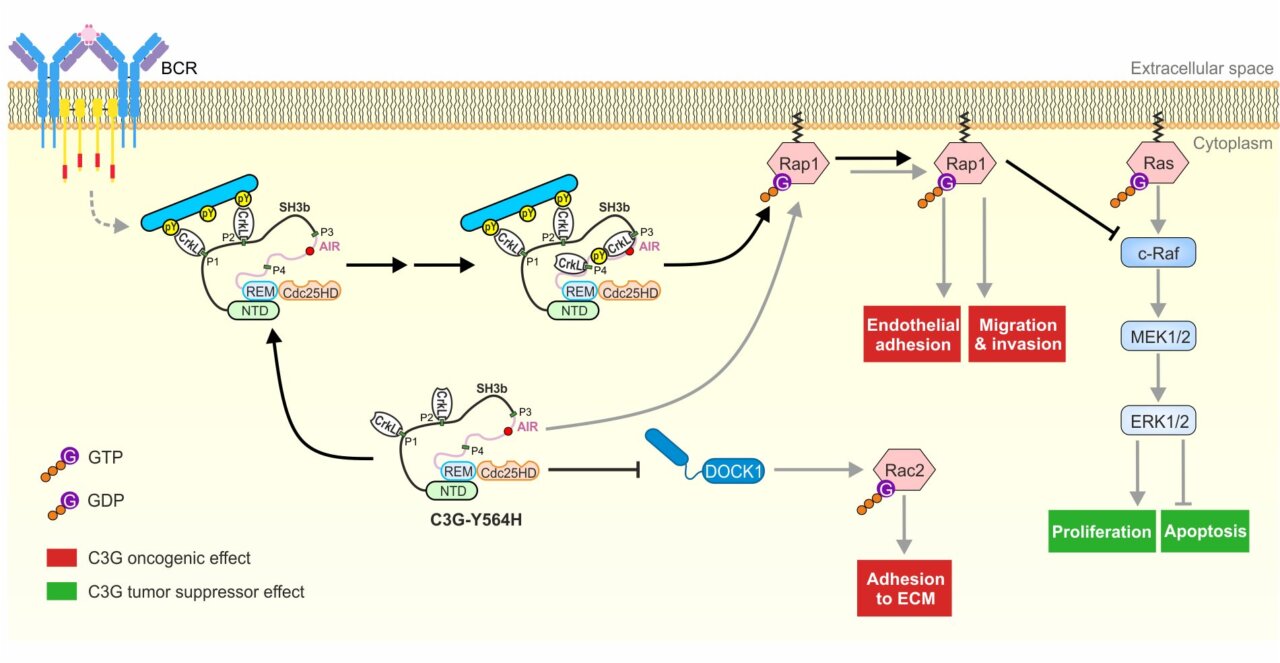
La proteína C3G (RapGEF1) funciona como un “interruptor” molecular que activa de forma controlada a Rap1, una molécula clave para que las células se adhieran, crezcan o se desplacen. Sin embargo, en algunos pacientes con linfoma no Hodgkin se ha identificado una mutación -denominada Y554H- que elimina su mecanismo de control y la mantiene permanentemente activa.
Para comprender sus efectos, el equipo recreó la mutación equivalente en ratón (Y564H) en células de linfoma mediante la herramienta de edición genética CRISPR. El objetivo: analizar cómo influye esta alteración en el comportamiento tumoral.
Menor crecimiento, pero mayor capacidad de escape
Los resultados en modelos celulares muestran que las células con la mutación C3G-Y564H presentan Rap1 activado de forma constante, tanto en reposo como tras estímulos habituales en las células B.
Esta hiperactivación tuvo un efecto claro: redujo la señal de crecimiento descontrolado al disminuir los niveles de c-Raf. Como consecuencia, las células mutadas crecieron hasta un 50 % menos en 72 horas, según mediciones realizadas por citometría y microscopía en tiempo real.
Además, estas células resultaron más vulnerables al estrés, al presentar menores niveles de Bcl-xL, una proteína que protege frente a la apoptosis (muerte celular programada).
Sin embargo, el mismo mecanismo que frena el crecimiento también altera la capacidad de adhesión. La mutación reduce la actividad de Rac2, proteína implicada en la unión de las células sanguíneas a su entorno. Las células mutadas se adhieren menos a proteínas como fibrinógeno y fibronectina, así como a células endoteliales (HUVEC), pero muestran mayor facilidad para migrar guiadas por señales químicas, con un aumento de hasta el 50 % en su capacidad de desplazamiento.
El análisis genético reveló miles de cambios asociados a procesos de movimiento y adhesión celular.
Confirmación en modelos animales
Para validar estos hallazgos en condiciones fisiológicas, los investigadores emplearon modelos animales. Inyectaron células tumorales A20 en ratones BALB/c inmunocompetentes y evaluaron la evolución de la enfermedad.
Tras 21 días, los animales que recibieron células con la mutación C3G-Y564H desarrollaron un mayor número de focos metastásicos en el hígado. Aunque estos focos eran de menor tamaño, resultaban más numerosos que en los controles.
Además, los clones con menor expresión de C3G mostraron una diseminación todavía mayor, lo que refuerza la idea de que esta proteína ejerce un doble papel en el linfoma B.
Alba Morán-Vaquero, primera firmante del estudio, subraya: “Los resultados in vivo confirman el doble efecto de C3G: actúa como supresor del crecimiento primario a través de Rap1, pero promueve la metástasis al inhibir Rac2 y reducir la adhesión celular”.